【Organic Chem.】烷烃alkane
分类:
是C和H两种元素组成,C与C均以单键相连的一大类化合物
Cn H(2n+2) 分为:链烷烃;环烷烃(脂环化合物)

烷烃
物理性质:
室温下,1-4 C 气体;5-16 液体,低沸点;17以上,固体。熔点不超过100摄氏度。【烷烃为非极性分子,偶极矩为0,分子中国呢的电荷分配不均匀,会产生瞬间偶极矩,存在色散力,此外还有 van der waals,克服这些作用力所需能量较低,因此有机化合物沸点不超过300摄氏度】
沸点 同分异构中 直链烷烃比叉链烷烃 高;叉链越多,沸点越低。【分子质量增加,分子间作用力增大,分子运动所需能量增大,所有沸点增高。。。叉链空间位阻作用,分子间作用力小,沸点低】
烷烃偶极矩为O 非极性分子,统一非极性溶液。不溶于水
构象:
二面角:相邻C的其他键,在以C-C键为轴旋转时,会交叉成一定的角度。旋转一周,会产生无数个旋转异构体,其中二面角0度为重叠性ecipsed;60度为交叉型 staggered.

重叠型C原子的H重叠,构象最不稳定,存在斥力;交叉型H原子距离远,能量上最稳定。
烷烃的反应:
化学键的断裂:
均裂(自由基)和易裂(离子型反应)
自由基反应: 断裂时,平均分给2量子或集团。自由基只有瞬间寿命,是活体中间体的一种。化学键两端元素电负性相当。
离子型反应: 断裂时,一对成键电子为某一院子或基团所占有。产生正负离子。瞬间寿命
协同反应:旧键断裂和新键生成在同一步骤完成。该反应很多通过环状过渡态完成。
反应性分析
烷烃只含有C-H C-C 都属于单键,需要较高的能量。因此烷烃具有极大的化学稳定性。会发生均裂产生自由基。
键的解离反应焓:室温下,分子处于基态,振幅很小,类似于弹簧连接的小球运动,吸收能量,振幅增大,到某一程度,键断裂。也是就键能 解离能。解离能越低,形成的C自由基越稳定。
热裂:无氧状态,高温下800摄氏度,发生C—C断裂。分子越大越容易断裂,热裂后的分子还可再进行特裂【石油变汽油】
烷烃的氧化
自动氧化
老化,老化过程很慢,空气中的氧与物质中具有活波H的各种分子发生自动氧化反应,继而在发生其他反应。人老化的皮肤等等。
燃烧
烷烃完全燃烧 生成CO2和水,同时释放大量热。
异构化
通常在催化剂作用下,从一个异构体转变成另一个
自由基取代反应
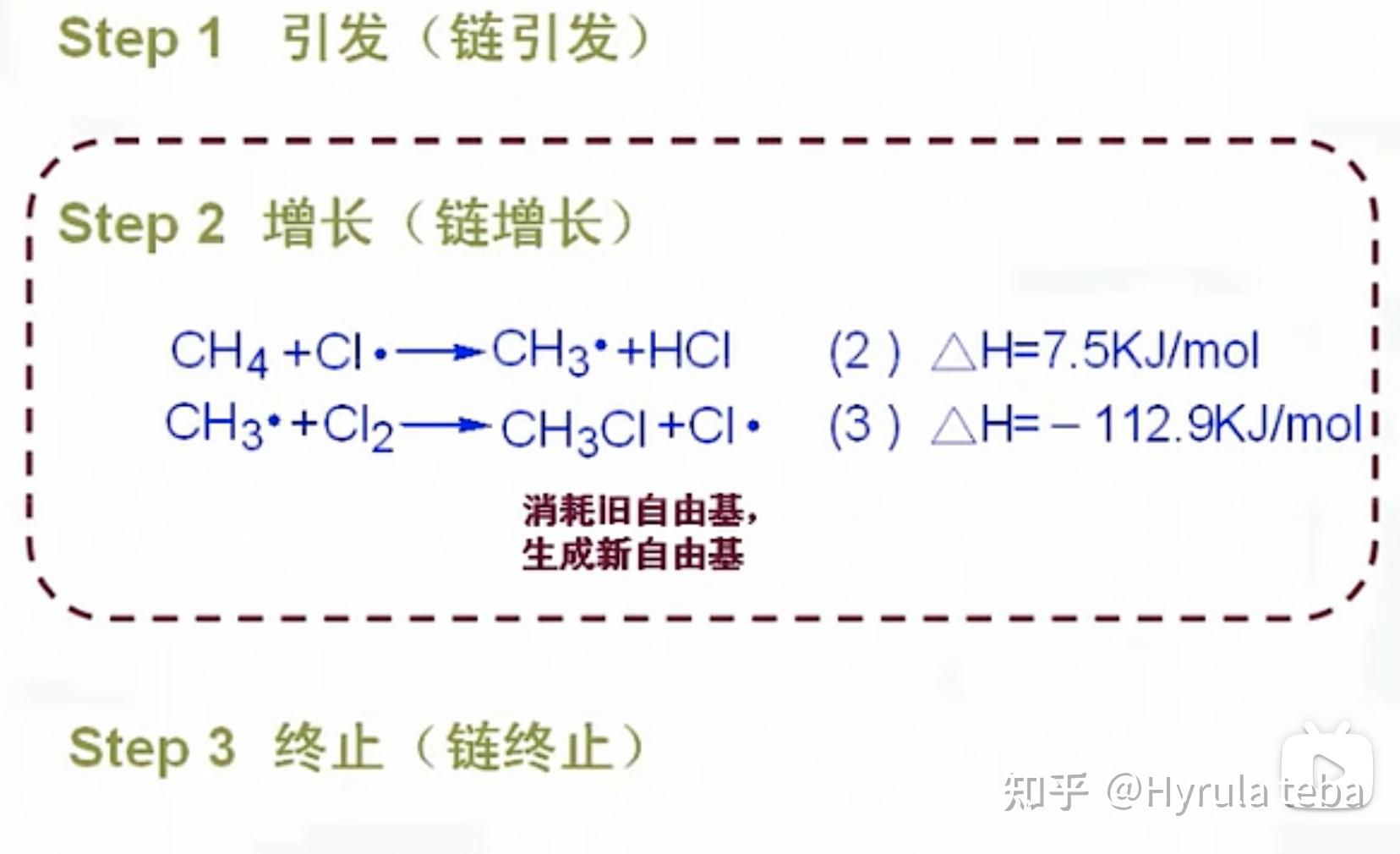
没有明显的溶剂效应,催化剂也没有明显影响,需要诱导期。一般都要经过链引发,链生长,链终止 三个阶段。
链引发 是产生自由基的阶段,键均裂需要吸收能量,所以需要加热或光照。

环烷烃
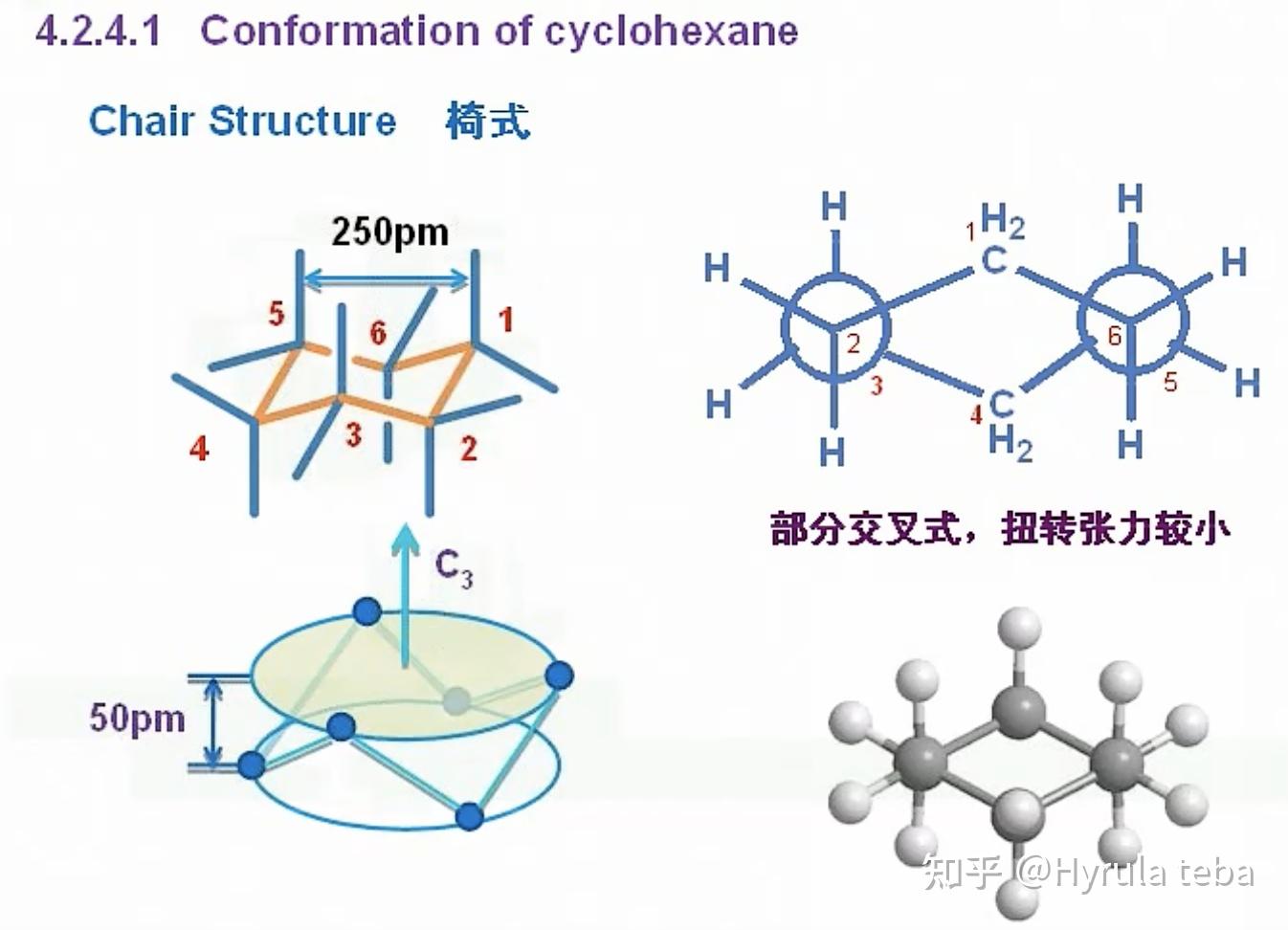
三元换和芳香型环系具有平面结构,其他环都不是真正的平面结构。6元环最为稳定。【结构一节会详细解析】
分类

命名
单环
- 支链不复杂以环为母体命名
- 支链复杂,以环烷为取代基
- 两环相连 大环为母体

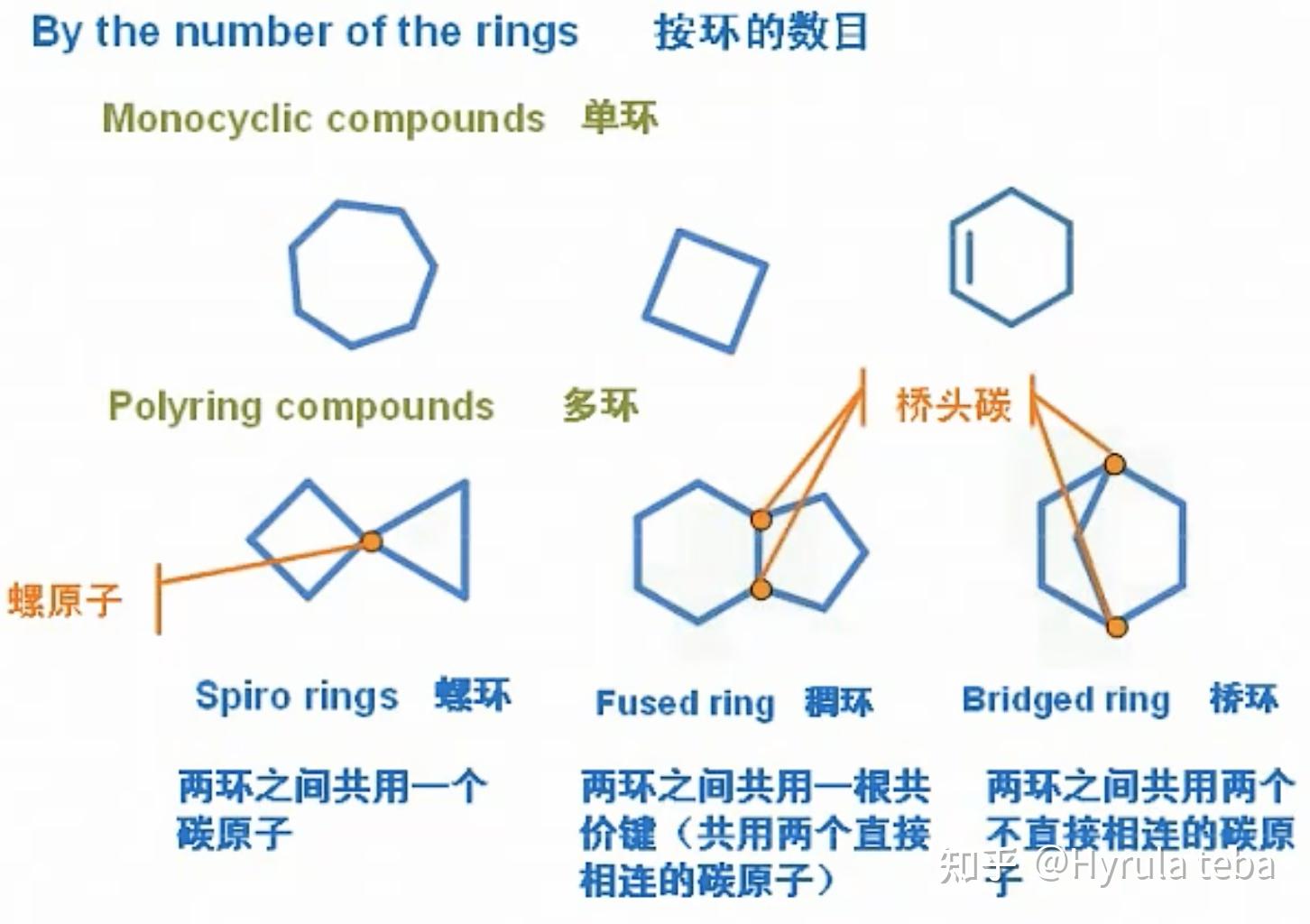
多环
螺环烃,取代基位号最小原则。

二环桥环和稠环

多元环

结构
bayer 张力学说【错误假说】
该假说认为所有的环状化合物都具有平面型正多边结构,C原子采用Sp3杂化键角为109度28分,举例:三元环内角为60度,由109压缩;7元环内角128,由109扩张。一位这化合物内部产生了张力。张力越大环越不稳定。
【该理论是事实不符,正确性存在问题】
稳定程度应该用燃烧热来判断,结果表面6元环最稳定。【燃烧热值需要平均到每个C原子上】
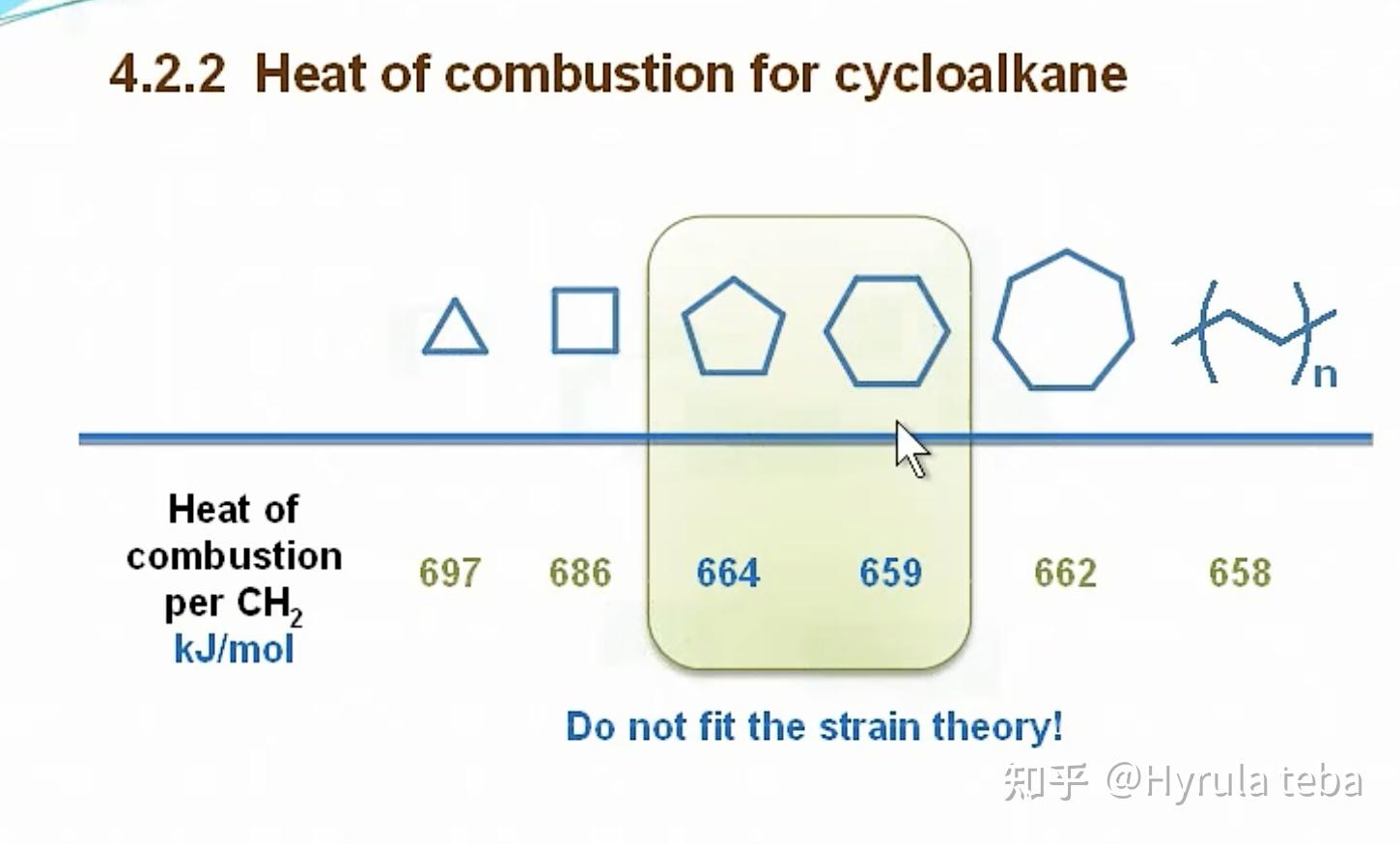
【正确】影响环体系稳定性的主要因素
- 环张力(Boyer)
- 扭转张力:重叠或交叉
- Van De Waals force


物理性质:
分子较规则,排列紧密;熔点沸点一般高于相应的直链烷烃
文章被以下专栏收录


